Krebspatienten zeigen aufgrund einer chronisch übersäuerten Stoffwechellage häufig schwere Symptome wie Dyspnoe (Atemnot) und Tachypnoe (beschleunigte Atmung) aber auch Muskelschwäche und einen insgesamt schlechten Allgemeinzustand. Klinisch imponiert besonders die Kussmaul-Atmung (erhöhte Atemtätigkeit Hyperventilation mit normaler Frequenz) mit starkem Unbehagen. Neben einem niedrigen pH-Wert wird bei erhöhten Laktatwerten häufig ein reduziertes Standard-Bikarbonat (normal: 22-26 mmol/l) und eine erhöhte Anionen-Lücke diagnostiziert. Eine Hypoglykämie (abnorm niedriger Blutzuckerspiegel) bei Laktat-Azidose ist klassisch, aber nicht immer vorhanden [6].
Laktat-Azidose durch Krebs
Tumorzellen verbrauchen große Mengen an Glucose. Sie metabolisieren Glucose trotz ausreichender Mengen an Sauerstoff und Nährstoffen bevorzugt durch Glykolyse (Warburg-Effekt). Dieser Stoffwechselweg ist zwar ineffizient, um ATP (Adenosintriphosphat) zu erzeugen, erleichtert aber primär die schnelle Aufnahme von Nährstoffen ins Tumorgewebe [2]. Die zahlreichen glykolytischen Zwischenprodukte können in Lipide, Nukleotide und Proteine umgewandelt werden, die essentielle Bestandteile von Krebszellen sind [3]. Milchsäure ist ein Nebenprodukt der Glykolyse und wird zu Laktat und einem Proton aufgespalten:
CH3-CHOH-COOH → CH3-CHOH-COO- + H+
Eine Laktat-Azidose (LA) bzw. Hyperlaktämie resultiert aus der systemischen Akkumulation von Laktat und Protonen aufgrund der erhöhten Umwandlung von Pyruvat zu Laktat durch das Enzym Laktatdehydrogenase (LDH). Krebszellen können, stimuliert durch eine Hypoxie (Sauerstoffmangel) [4], aufgrund einer erhöhten Glykolyserate Laktate in großen Mengen erzeugen. Viele Faktoren können zu der hohen Geschwindigkeit der Glykolyse beitragen, insbesondere eine abweichende Expression oder Überexpression von glykolytischen Enzymen, wie z. B. der Hexokinase.
Bikarbonat-Therapie bei Karzinomen
Laktate werden in der Leber und in den Nieren metabolisiert und eliminiert. Daher können Leber- oder Niereninsuffizienz zur Entstehung einer Laktat-Azidose beitragen. Die Elimination durch eine aktive Laktat-Sekretion über die Nieren oder die Metabolisierung durch Glukoneogenese (Zuckerneubildung ) in der Leber können die tumorinduzierte erhöhte Produktion häufig nicht kompensieren [5]. Dann erhalten die Patienten mit schwerer metabolischer Azidose unabhängig von der Ätiologie häufig intravenöses Bikarbonat als primäre Akutbehandlung, um die Säure-Last zu reduzieren und die Laborparameter (Blut-pH, Standard-Bikarbonat, Anionen-Lücke) zu normalisieren. Ergänzend kann eine Hämodialyse Laktate effizient aus dem Blut eliminieren. Ziel ist es, den Patienten möglichst schnell zu stabilisieren, bevor eine Chemotherapie durchgeführt werden kann.
Die Studie von Gillies, Ibrahim-Hashim, Ordway und Gatenby [16] konzentriert sich auf die Rolle von Alkalisierungsmitteln bei Krebs. Ein dysregulierter Stoffwechsel, zu dem auch der Warburg-Effekt gehört, ist ein Merkmal von Krebszellen, das zu einer erhöhten Säureproduktion und einer Anhäufung von Protonen im Interstitialraum führt. Die krebsbedingte Übersäuerung der Mikroumgebung stellt eine Strategie zum Aufbau von Nischen dar, um die Proliferation von Krebszellen zu fördern. Zu den ökologischen Vorteilen, die eine Krebspopulation dadurch erhält, gehören die Umgestaltung der extrazellulären Matrix zur Förderung der lokalen Invasion, die Unterdrückung der potenziell konkurrierenden Proliferation von Fibroblasten und die Unterdrückung der Immunantwort. Präklinische Daten zeigen, dass eine Erhöhung der Pufferkapazität des Serums die saure Mikroumgebung des Tumors neutralisieren und die lokale Invasion und Proliferation hemmen kann, was synergistisch zu den Wirkungen von Chemo- und Immuntherapeutika wirken kann. In der Studie wird auch die gezielte Bekämpfung der Tumorazidose mit alkalisierenden Mitteln erörtert, einschließlich der Ergebnisse der klinischen Bikarbonatstudie.
Laktate bei Tumorerkrankungen
Yasumasa Kato und sein wissenschaftliches Team beschreiben in ihrer Studie zum Krebsmetabolismus den Zusammenhang von Laktaten und Tumoren [4]. Dabei kamen sie zu folgenden wichtigen Ergebnissen:
- Eine chronische metabolische Laktatazidose kann zur Tumorprogression führen und die Malignität des Tumors erhöhen.
- Ein niedriger Laktatspiegel kann die Überlebenszeit von Krebspatienten (bei Kopf- und Halstumoren) verbessern.
- Eine Hemmung des Laktatrezeptors GPR81 kann Tumorwachstum und Metastasierung hemmen.
- Eine chronische Laktatazidose kann zu Rezidiven führen.
Niedriger Extrazellulärer pH (pHe) fördert Invasion und Metastasierung von Krebszellen
Eine extrazelluläre Azidose in der Mikroumgebung des Tumors wird durch die Aktivität der Carboanhydrase IX aufrecht erhalten. Dadurch entsteht ein saures Milieu, das von Krebszellen toleriert wird und zur Entwicklung eines metastatischen Phänotyps beiträgt und insgesamt die weitere Invasion und Metastasierung fördert. Zusätzlich triggert ein niedriger pHe den Calcium-Einfluss in die Krebszellen, was mit einer erhöhten Resistenz gegen Krebsmedikamente asasoziiert ist, und erhöht die Radikal-Bildung, was mit einer erhöhten Metastasierung assoziiert ist [4].
Der extrazelluläre pH-Wert solider Tumore ist wegen der hohen Produktionrate an Laktat (eine Konsequenz des fermentativen glykolytischen Stoffwechsels) und aufgrund der schlechten Durchblutung eindeutig sauer. Die Azidität trägt zur Tumorprogression bei, indem sie eine Genominstabilität induziert sowie die lokale Invasion und Metastasen fördert, die Anti-Tumor-Immunität inhibiert und zu einer Resistenz gegen Chemo- und Radiotherapien führt. Systemische Puffer-Behandlungen können die Tumorazidität neutralisieren, die lokale Invasion und Metastasierung hemmen und die Immunüberwachung in verschiedenen Krebs-Modellsystemen verbessern [11].
Orale Bikarbonat-Gabe bei Krebs
Eine adjuvante Therapie mit Natriumbikarbonat ist in verschiedenen Stadien einer Krebstherapie sinnvoll. Zunächst ist sie essentiell, um bei einer manifesten Laktatazidose die primären Parameter Blut-pH-Wert, Standard-Bikarbonat und Anionen-Lücke zu normalisieren und auf diese Weise den Patienten zu stabilisieren. Nur dann kann rasch eine Chemotherapie initiiert werden. Im weiteren Verlauf kann eine prophylaktische Gabe von oralem magensaftresistentem Natriumbikarbonat die Bikarbonatspeicher auffüllen und bei Wiederaufflammen der tumorösen Aktivität den erhöhten Verbrauch durch die anfallende Säure-Last kompensieren. Dadurch kann eine Azidose-Symptomatik vermieden und Zeit für die Initiierung einer Chemotherapie gewonnen werden.
Darüber hinaus konnte eine Studie im Computermodell zeigen, dass eine orale Gabe von Natriumbikarbonat den pH-Wert des Tumors und des umgebenden Gewebes anheben kann. Daraus folgern die Autoren, dass auf diese Weise das Tumorwachstum und die weitere Invasion gehemmt werden können [7]. Weitere Hinweise für die positiven Effekte von oralem Natriumbikarbonat bei Turmorerkrankungen konnten im Mausmodell dokumentiert werden. Die Arbeitsgruppe von Robey konnte zeigen, dass wahrscheinlich durch die Anhebung des extrazellulären tumoralen pH-Werts die Bildung von spontanen Metastasen bei Brustkrebs reduziert werden kann [8].
Azidose erhöht Krebs- und Sterberisiko
Diverse aktuelle Forschungsarbeiten deuten darauf hin, dass eine regelmäßige Kontrolle der Bikarbonat-Spiegel auch bei onkologischen Erkrankungen sinnvoll ist, um bei einer chronischen metabolischen Azidose (cmA) frühzeitig eine Therapie einzuleiten und Sicherheit bei der Titration zu erhalten.
In einer Studie wurde die Assoziation zwischen der Bikarbonat-Konzentration und der Mortalität in der Allgemeinbevölkerung untersucht. Insgesamt 31.195 Personen wurden durchschnittlich 6,7 Jahre begleitet. Von den 2.798 verstorbenen Patienten, waren bei 722 kardiovaskuläre Krankheiten und bei 620 Krebserkrankungen die Todesursachen. Verglichen mit den Teilnehmern, bei denen die Serum-Bikarbonat-Level 22-26 mmol/l betrugen, hatten die Patienten mit einer cmA < 22 mmol/l ein erhöhtes Gesamtmortalitäts-Risiko und ein erhöhtes Risiko für eine krebsbedingte Sterblichkeit [9].
Es gibt neuere Hinweise für eine Verbindung zwischen niedrigen Serum-Bikarbonat-, tumoralen pH-Werten und einer krebsbedingten Entzündung. Von insgesamt 3.281 Darmkrebspatienten, die sich einer Tumorresektion unterzogen haben, gab es von 2.223 Probanden, die sich in den Stadien I-IV befanden, verfügbare Analysedaten. Die australischen Wissenschaftler stellten fest, dass die Serum-Bikarbonatspiegel in einer multivariaten Analyse mit der peri-operativen Mortalität assoziiert waren. Für das langfristige Überleben von 5 Jahren war Bikarbonat signifikant mit der Gesamtüberlebenszeit in einer univariaten, jedoch nicht signifikant in einer multivariaten Analyse assoziiert. In einer explorativen Analyse waren die Serum-Bikarbonat-Konzentrationen signifikant mit dem Lymphozyten zu Monozyten-Verhältnis und dem Neutrophilen zu Lymphozyten-Verhältnis verbunden. Fazit: Bei peri-operativen Darmkrebspatienten, waren die Serum-Bikarbonat-Spiegel mit einer 30-tägigen Überlebenszeit, nicht jedoch mit einer Fünf-Jahres-Überlebenszeit assoziiert [10].
Bikarbonat verlängert die Überlebenszeit bei Pankreaskarzinom
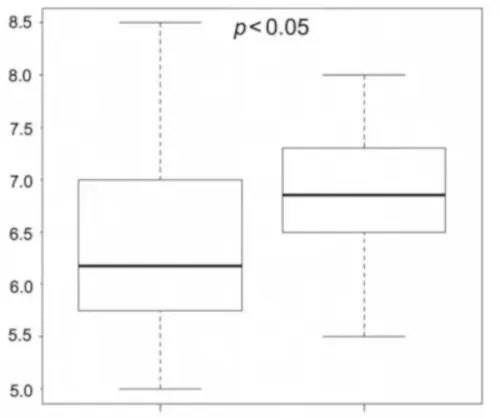
In einer japanischen Studie erhielten Patienten mit metastasierten oder rezidivierenden Pankreaskarzinomen gleichzeitig zur Chemotherapie eine Alkalisierungsbehandlung, bestehend aus einer alkalischen Ernährung und einer Supplementierung mit oralem Natriumbikarbonat (3 bis 5 g/d). Der durchschnittliche Urin-pH-Wert war nach der Alkalisierungstherapie signifikant höher. Von Beginn der Alkalisierungsbehandlung an hatten Patienten mit einem hohen Urin-pH-Wert (> 7) eine signifikant längere mediane Gesamtüberlebenszeit, als die Erkrankten mit niedrigen Konzentrationen (<= 7) [12].
Gesamtüberleben: Das mediane Gesamtüberleben ab dem Zeitpunkt der Diagnose oder des Rezidivs war in der Alkalisierungsgruppe signifikant länger als in der Kontrollgruppe [Alkalisierungsgruppe: n=36, 15,4 Monate, 95% Konfidenzintervall (CI)=10,2-24,7 vs. Kontrollgruppe: n=89, 10,8 Monate, 95% CI=8,7-12,3; p<0,005]. Das mediane Gesamtüberleben von Patienten mit einem Urin-pH-Wert von über 7,0 in der Alkalisierungsgruppe betrug 25,1 Monate [n=13, 95% CI=5,2-nicht anwendbar (NA)] im Vergleich zu 10,8 Monaten bei Patienten in der Kontrollgruppe (n=89, 95% CI=8,7-12,3; p<0,005)). Das mediane Gesamtüberleben der Patienten mit einem Urin-ΔpH von mehr als 1,0 in der Alkalisierungsgruppe betrug 19,8 Monate (n=10, 95% CI=6,1-NA) im Vergleich zu 10,8 Monaten für Patienten in der Kontrollgruppe (n=89, 95% CI=8,7-12,3; p<0,05). Zwanzig der 36 Patienten in der Alkalisierungsgruppe sind bis zum 31. Dezember 2019 verstorben, während 71 der 89 Patienten in der Kontrollgruppe bis zum 30. November 2017 verstorben sind.
Alkalisierung mit Bikarbonat unterstützt Chemotherapie
SN-38, ein aktiver Irinotecan-Metabolit, wird vom Intestinaltrakt während der Ausscheidung reabsorbiert, was eine Diarrhö und Neutropenie verursacht. Eine schnelle Exkretion von SN-38 soll dagegen eine Neutropenie verhindern. Orale Arzneimittel zur Alkalisierung werden als vorbeugende Mittel genutzt, um die SN-38-Wiederaufnahme zu unterdrücken. In einer japanischen Studie wurde Patienten mit Gebärmutterhals- und Eierstockkrebs Irinotecan und eine orale Medikamentenkombination aus Ursodeoxycholsäure, Magnesiumoxid und Natriumbikarbonat verabreicht. Die Alkalisierungstherapie verbesserte signifikant die Anzahl an Neutrophilen und reduzierte die Dosisintensität im Vergleich zu den Probanden, die keine Alkalisierungsbehandlung erhielten. In der umfangreichen japanischen Datenbank über unerwünschte Arzneimittelnebenwirkungen war die Wahrscheinlichkeit einer Irinotecan-induzierten Neutropenie signifikant geringer, wenn die Substanz in Kombination mit oralen alkalisierenden Medikamenten gegeben wurde [13].
Intravenöses Natriumbikarbonat wird normalerweise in Alkalisierungsregimen zur sicheren Anwendung von hoch dosiertem Methotrexat (HDMTX) eingesetzt. Es gab aber auch schon Engpässe an Natriumbikarbonat zu i.V.-Zwecken. Die Frage war nun, ob orales Natriumbikarbonat ähnliche Effekte erzielen kann. Urinparameter, einschließlich Urinproduktion und pH-Wert, sind wichtig um das Risiko eines Nierenschadens zu minimieren, der die Nebenwirkungen und Länge des Krankenhausaufenthaltes nach HDMTX erhöht. In einer prospektiven US-amerikanischen Studie erhielten Patienten mit Non-Hodgkin-Lymphomen und akuter lymphoblastischer Leukämie HDMTX und ein orales Regime aus Natriumbikarbonat und Acetazolamid (ein Sulfonamid mit diuretischer Wirkung) um einen Urin-pH-Wert von > 7 zu erreichen. Die Kohorte wurde anschließend mit einer Kontrollgruppe verglichen, die intravenöses Natriumbikarbonat bekam. Es zeigten sich weder Unterschiede zwischen dem oralen und dem intravenösen Alkalisierungsregime in Bezug auf die Inzidenz einer akuten Niereninsuffizienz, noch Unterschiede bei der MTX-Clearance zwischen beiden Regimen. Orales Natriumbikarbonat kann demnach durchaus eine Option sein, falls es wieder mal Engpässe mit der Substanz zu i. V. Zwecken gibt [14].
Bei Neoblasenkonstruktion Bikarbonat-Therapie
In einer deutsch-US-amerikanischen Studie haben sich 345 Patienten nach einer radikalen Harnblasen-Entfernung (Zystektomie) und einer Ileum-Neoblasenkonstruktion wegen eines Harnblasen-Karzinoms einer dreiwöchigen stationären Rehabilitation unterzogen [15]. Je nach Art und Länge des ausgeschalteten Darmsegments zwecks Harnableitung kann eine metabolische Azidose auftreten. Daher ist bei der Nachsorge auf die Anfertigung einer Blutgasanalyse (BGA) zu achten. Zu Beginn der Reha, durchschnittlich 29 Tage nach der Operation, hatten 200 Patienten (58 Prozent) eine metabolische Azidose.
Während des Rehazeitraums nahm der Bedarf an oralem Natriumbikarbonat-Ersatz aufgrund einer Azidose signifikant von 45,2 Prozent auf 86,7 Prozent zu, während die Harninkontinenz signifikant abnahm. Eine verminderte Harninkontinenz wurde als unabhängiger Risikofaktor für eine metabolische Azidose identifiziert.
Fazit: Das Risiko einer metabolischen Azidose nach einer Neoblasenkonstruktion korrelierte mit einer kontinuierlich besseren Kontinenz in der frühen Regenerationsphase. Daher sollte der Säure-Basen-Status in diesem Zeitraum häufiger bestimmt werden, um eine metabolische Azidose zu erkennen. Der mediane Basenüberschuss war am Ende der Reha im Normbereich [15].
Fazit
Bei Krebspatienten sollte auch der Säure-Basen-Status im Fokus stehen. Denn niedrige Serum-Bikarbonat-Werte werden mit einer systemischen Entzündung assoziiert, die auch ein Kennzeichen von Krebserkrankungen ist. Die Azidität trägt u. a. zur Tumorprogression bei und begünstigt die Resistenz gegen Chemo- und Radiotherapien. Alkalisierungstherapien können zudem die Nebenwirkungen bestimmter Zytostatika lindern. Optimal ist ein stets ausgeglichener Säure-Basen-Haushalt mit einem Standard-Bikarbonat in der Blutgasanalyse (BGA) zwischen 22 mmol/l und höchstens 26 mmol/l. Die kontrollierte Einnahme von magensaftresistentem Natriumbikarbonat mit hoher Bioverfügbarkeit ist für den Säure-Basen-Ausgleich besonders geeignet und wird von Experten empfohlen.


 Die Nierenfunktion nimmt natürlicherweise mit zunehmendem Alter ab. Dadurch kann es zu einer Übersäuerung des Körpers und einer zusätzlichen Schädigung des Nierengewebes kommen. Die damit verbundenen Beschwerden reichen von Osteoporose und Muskelschwund bis zu einem Vitamin B12-Mangel.
Die Nierenfunktion nimmt natürlicherweise mit zunehmendem Alter ab. Dadurch kann es zu einer Übersäuerung des Körpers und einer zusätzlichen Schädigung des Nierengewebes kommen. Die damit verbundenen Beschwerden reichen von Osteoporose und Muskelschwund bis zu einem Vitamin B12-Mangel.